EPICE
Wat?
Effective Perinatal Intensive Care in Europe – Effectieve Perinatale Intensieve Zorg in Europa

Achtergrond
Extreem of ernstig/zeer prematuur geboren kinderen (vóór 32 weken zwangerschap) zijn slechts 1 of 2% van alle geboorten, maar deze kwetsbare groep vormt de helft van alle sterfgevallen tijdens het eerste levensjaar.1,2 Vergeleken met baby’s die na een voldragen zwan-gerschap zijn geboren, worden deze kinderen vaker geconfronteerd met hogere risico’s inzake gezondheidsproblemen en ontwikkelings-achterstanden gedurende de kindertijd.2–4 In Europa zijn er verschillen tussen de landen met betrekking tot sterfte en ernstige neonatale gezondheidscomplicaties bij extreem of ernstig/zeer prematuur geboren kinderen (vóór 32 weken zwangerschap).5 Redenen voor deze variatie kunnen deels verband houden met individuele kenmerken (de mate van vroeggeboorte of aanwezigheid van andere problemen zoals aangeboren misvormingen of slechte intra-uteriene groei), maar ook met de zorg voor deze baby’s, inclusief de organisatie van gezondheidszorgdiensten6 en het gebruik van evidence-based effectieve behandelingen in kraam- en neonatale afdelingen.
- WHO | Preterm birth. WHO. http://www.who.int/mediacentre/factsheets/fs363/en/. Accessed January 31, 2018.
- Althabe F, Howson CP, Kinney M, Lawn J, World Health Organization. Born Too Soon: The Global Action Report on Preterm Birth.; 2012. http://www.who.int/pmnch/media/news/2012/201204%5Fborntoosoon-report.pdf. Accessed January 31, 2018.
- MacDorman MF, Matthews TJ, Mohangoo AD, Zeitlin J. International comparisons of infant mortality and related factors: United States and Europe, 2010. Natl Vital Stat Rep Cent Dis Control Prev Natl Cent Health Stat Natl Vital Stat Syst. 2014;63(5):1-6.
- Saigal S, Doyle LW. An overview of mortality and sequelae of preterm birth from infancy to adulthood. Lancet Lond Engl. 2008;371(9608):261-269. doi:10.1016/S0140-6736(08)60136-1
- Blencowe H, Cousens S, Oestergaard MZ, et al. National, regional, and worldwide estimates of preterm birth rates in the year 2010 with time trends since 1990 for selected countries: a systematic analysis and implications. The Lancet. 2012;379(9832):2162–2172.
- Papanicolas I, European Observatory on Health Systems and Policies, eds. Health System Performance Comparison: An Agenda for Policy, Information and Research. Maidenhead, Berkshire, England: Open University Press; 2013.
Structuur
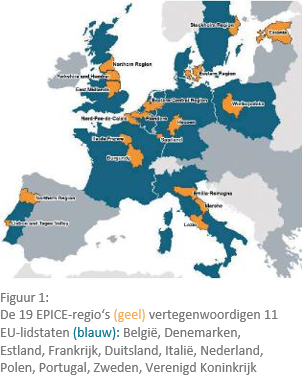
In het EPICE-project (Effective Perinatal Intensive Care in Europe, Effectieve Perinatale Intensieve Zorgen in Europa) onderzocht een onderzoeksgroep (consortium) het gebruik van evidence-based*[1] interventies in de zorg van extreem of ernstig/zeer premature baby’s in 19 regio’s uit 11 EU-lidstaten (figuur 1). Gegevens werden verzameld gedurende een periode van 12 maanden in elke regio (behalve Frankrijk tot 6 maanden) van april 2011 tot september 2012. In totaal werden 10.369 geboortes van 22 tot 31 voltooide zwangerschapsweken (levendgeborenen, doodgeborenen) en 335 kraamafdelingen alsook 242 neonatale afdelingen opgenomen in de analyse. De multi-disciplinaire aanpak brengt expertise samen in verloskunde, kindergeneeskunde, epidemiologie, biostatistiek en onderzoek naar gezondheidszorgdiensten.
[1] Evidence-based verwijst naar behandelingen die gebaseerd zijn op resultaten van systematisch onderzoek in plaats van dat deze enkel gebaseerd zijn op de mening van deskundigen of de gebruikelijke praktijk.
Primaire onderzoeksvragen
Krijgen alle extreem extreem of ernstig/zeer prematuurvroeg geboren baby’s in Europa ultramoderne bewezen effectieve evidence-based zorg?
Draagt evidence-based zorg bij aan verschillen in sterfte en problemen met de gezondheid?
Welke zijn de faciliterende en belemmerende factoren om evidence-based effectieve zorg en de beste klinische behandelingen in neonatale intensive care-afdelingen te implementeren.
Gegevensverzameling methoden
Het EPICE-project omvatte 4 verschillende gerelateerde studies. Binnen deze studies werd een breed scala aan hulpmiddelen gebruikt om kwantitatieve en kwalitatieve*[1] gegevens te verzamelen na geïnformeerde toestemming van de ouders. Deze aanpak helpt om een beter inzicht te verkrijgen in het gebruik van evidence-based effectieve zorg op patiënt-, afdeling- en regionaal niveau.
[1] Kwantitatief onderzoek is gericht op het meten van het probleem. Gegevens worden omgezet in getallen en in bruikbare statistieken om resultaten van doorgaans veel deelnemers te veralgemenen. Kwalitatief onderzoek wordt gebruikt om een grondig zicht te krijgen op de onderliggende redenen, meningen, gevoelens en motivaties en wordt uitgevoerd met behulp van individuele persoonlijke interviews, focusgroepen (groepsdiscussies) of zelfs directe meting van gedrag.
Op populatie gebaseerde prospectieve cohortstudie[1] van alle extreem of ernstig/zeer premature doodgeboortes en geboortes van 22 tot 32weken zwangerschap om gegevens te verzamelen over medische praktijken, klinische kenmerken en gezondheidsresultaten tot 2 jaar
- Medische dossiers om gegevens te verzamelen over medische behandelingen, klinische kenmerken en gezondheidsresultaten
- Vragenlijsten voor ouders
[1] Een type onderzoek waarbij deelnemers worden gerekruteerd en gedurende een tijd worden gevolgd (hier: om de gevolgen van prematuriteit na te gaan)
Enquête voor de afdelingen verloskunde en neonatologie over structurele kenmerken, beleid, protocollen en behandelingen
- Vragenlijsten voor de afdeling verloskunde
- Vragenlijsten voor de afdeling neonatologie
Kwalitatief onderzoek in geselecteerde afdelingen over factoren die het doorvoeren van evidence-based effectieve behandelingen remmen of juist vergemakkelijken.
- Semi-gestructureerde interviews en focusgroepen met kinderarts-neonatologen en verpleegkundigen
Case studies over regionale, nationale, Europese en internationale overheidsstructuren
- Document analyse
Onderzochte evidence-based behandelingen
Om een breder zicht te krijgen op het gebruik van evidence-based effectieve behandelingen bij de verzorging van extreem of ernstig/zeer premature baby’s, heeft het EPICE-consortium overeenstemming bereikt over 17 behandelingen met betrekking tot zowel verloskundige als neonatale zorg om in het project te worden opgenomen. Deze interventies (zie vakjes) werden geselecteerd op basis van de volgende criteria:
De interventie heeft een significante impact op gezondheid en/of wordt algemeen toegepast
Er is een hoog niveau van bewijs voor het gebruik of niet-gebruik van de interventie
Vergelijkbare indicatoren:
de interventie kan op dezelfde manier worden gemeten in alle deelnemende afdelingen
Er bestaan verschillen tussen regio’s en afdelingen, hetgeen suggereert dat niet-klinische factoren zoals de organisatie van zorg- of verstrekkerskenmerken een impact hebben
Vóór de geboorte (antenataal)
- Toediening van antibiotica (om vroegtijdige weeën te verminderen)
- Tocolyse-toediening van weeënremmers (om vroegtijdige bevalling te onderdrukken)
- Toediening van corticosteroïden vóór de geboorte (om de rijping van de longen van de baby te verbeteren)**
- Toediening van magnesiumsulfaat voor neuroprotectie (bescherming tegen hersenbeschadiging) (bijvoorbeeld om het risico op hersenverlamming / hersenbeschadiging bij de baby te verminderen)
Rond de geboorte (perinataal)
- Bevalling in kraamafdelingen met bijbehorende lokale neonatale intensive care**
- Optimale bevallingsmethode voor extreem of ernstig/zeer premature baby’s
- Timing van navelstrengafklemming (laat klemmen verhoogt het bloedvolume van de baby en vermindert het risico op hersenbloeding) **
- Preventie van lage lichaamstemperatuur (hypothermie/onderkoeling) **
- Surfactant*[1]-toediening (om ademhalingsinsufficiëntie te voorkomen)**
Na de geboorte (postnataal)
Management van de open ductus arteriosus (het korte vat dat de longslagader verbindt met de aorta-lichaamsslagader, en SOMS open blijft na de vroeggeboorte)
- Inhalatie van stikstofmonoxide (om bronchopulmonale dysplasie (BPD) te voorkomen)
- Niet-gebruik van corticosteroïden na de geboorte (deze werden veel gebruikt voor de behandeling en preventie van BPD bij premature baby’s totdat studies op een verhoogd risico wezen op hersenverlamming en neurologische ontwikkelingsstoornissen)**
- Strategieën ter voorkoming van bronchopulmonale dysplasie (BPD)
- Screening en behandeling van retinopathie van prematuren (ROP) (teveel zuurstof kan ervoor zorgen dat abnormale bloedvaten in het netvlies groeien en dit kan tot blindheid leiden) **
- Toediening van probiotica*[2] (om het risico op necrotiserende enterocolitis (NEC) te verminderen; NEC is een zeldzame maar ernstige darmaandoening met een hoog sterftecijfer)
- Borstvoeding en gebruik moedermelk **
- Huid-op-huid contact / kangoeroeën (direct huidcontact tussen moeder en baby, kan vader of ander familielid omvatten)
[1] Een natuurlijk geproduceerde stof die belangrijk is voor de functie van de longen. Foetussen ontwikkelen surfactant vanaf de 24e week van de zwangerschap, en dit bouwt op tot het volledige niveau tegen de 37e week van de zwangerschap.
[2] Levende bacteriën en gisten die goed zijn voor het spijsverteringskanaal en dus ook voor het immuunsysteem.
Resultaten
Krijgen alle extreem vroeggeboren baby’s in Europa ultramoderne wetenschappelijk evidence-based effectieve zorg?
- De studie identificeerde eerst 4 algemeen aanvaarde evidence-based behandelingen die de overleving van extreem of ernstig/zeer premature baby’s verbeteren: bevalling in een gespecialiseerde kraamafdeling met on-site neonatale intensive care-afdeling, toediening van prenatale steroïden om de foetale longrijping te bevorderen, preventie van onderkoeling na de geboorte en optimaal ademhalingsmanagement (gebruik van surfactant of vroege CPAP*[1]) bij de geboorte.
- Over de onderzoeksregio’s ontving slechts 58,3% van de baby’s al deze geselecteerde evidence-based behandelingen waarvoor ze in aanmerking kwamen.
- Baby’s geboren na een kortere zwangerschapsduur, groeiachterstand, lagere Apgar-scores*[2] ontvingen minder vaak deze evidence-based effectieve behandelingen.
Andere voorbeelden:
Het project heeft ook andere, evidence-based behandelingen onderzocht en vastgesteld dat niet-optimaal gebruik ervan veel voorkomt:
Gebruik van postnatale corticosteroïden bij te vroeg geboren baby’s
Postnatale corticosteroïden verhogen het risico op hersenverlamming en neurologische ontwikkelingsstoornissen bij kinderen die extreem of ernstig/zeer prematuur geboren zijn en daarom zijn richtlijnen voor beste behandelingen vereist voor beperkt gebruik van deze behandeling. Het EPICE-project toonde aan dat postnatale corticosteroïden nog steeds veel worden gebruikt in Europa, maar met een grote regionale variabiliteit die niet werd verklaard door de kenmerken van pasgeboren baby’s. Het hebben van een afdelingsbeleid om de toediening van corticosteroïden te beperken, droeg bij tot een lager gebruik en deze bevinding benadrukt het belang van richtlijnen om het gebruik van evidence-based behandelingen te stimuleren.
Borstvoeding
Borstvoeding is geassocieerd met lagere kans op overlijden bij extreem of ernstig/zeer premature baby’s en is gunstig voor de gezondheid van de moeder. De EPICE-groep analyseerde het verband tussen moeder-, verloskundige en kind-factoren (bijvoorbeeld type geboorte), opleiding van de moeder, het beleid van neonatologie en verloskundige afdelingen en moedermelkvoeding bij ontslag uit de NICU. In totaal ontving 58% van de baby’s moedermelk bij ontslag, maar er waren grote verschillen tussen regio’s (bereik 36-80%). Afdelingen met een Baby Vriendelijk Ziekenhuis-accreditatie en protocollen voor het gebruik van borst- en donormelk hadden een hoger percentage van exclusieve moedermelk voeding bij ontslag van de afdeling. Moeders met een hoger opleidingsniveau gaven vaker borstvoeding tot aan ontslag uit de NICU. In functie van de bewezen voordelen van moedermelk, moeten strategieën ter ondersteuning van borstvoeding ook gericht zijn op moeders met een lager opleidingsniveau.
Toediening van magnesiumsulfaat
Magnesiumsulfaat wordt al lang gebruikt in de verloskunde om zwangerschapsvergiftiging te voorkomen maar het werkt ook als een middel ter voorkoming van hersenschade voor de baby. Recente richtlijnen voor beste behandelingen stimuleren het gebruik van magnesiumsulfaat ter bescherming van de hersenen wanneer de geboorte van een extreem of ernstig/zeer premature baby wordt verwacht.
Het EPICE-consortium onderzocht het afdelingsbeleid van het gebruik van magnesiumsulfaat en het daadwerkelijke gebruik in Europese verloskundige afdelingen. Uit deze studie bleek dat het gebruik van magnesiumsulfaat voor neuroprotectie nog steeds zeldzaam was in Europa. De reden hiervoor kan zijn dat Europese gynaecologen niet overtuigd zijn door de beschikbare gegevens over het beschermende effect van magnesiumsulfaat op het voorkomen van hersenschade. Daarom is meer informatie uit onderzoeken nodig om te voldoen aan de nationale richtlijnen voor het gebruik van magnesiumsulfaat ter bescherming van de hersenen.
[1] Continuous Positive Airway Pressure: een ademhalings-ondersteunende methode die een constante stroom van lucht in de longen van de baby levert om de longblaasjes open te houden na elke ademhaling
[2] een methode om snel de gezondheid van een kind te bepalen door de pasgeboren baby direct na de geboorte te evalueren op vijf eenvoudige criteria: Ademhaling, Pols-/hartslag, Spierspanning/tonus, Aspect/kleur, Reactie op prikkels
Draagt toepassen van wetenschappelijk evidence-based zorg bij aan verschillen in sterfte en gezondheidsproblemen?
Gegevens van het EPICE-project tonen grote verschillen in percentages van vroeggeboorte, sterftecijfers (bijv. doodgeboorten, overleving tot ontslag van de afdeling), korte termijn-morbiditeit (frequentie van ziekten of complicaties) en ontwikkeling op langere termijn voor extreem of ernstig/zeer premature baby’s in de studiegebieden. Deze verschillen konden echter slechts in geringe mate worden verklaard door kenmerken van zwangerschap, moeder of baby.
Baby’s die alle 4 geselecteerde evidence-based effectieve behandelingen ontvingen, hadden 28% minder kans om te overlijden.
Als alle baby’s alle 4 geselecteerde evidence-based effectieve behandelingen zouden ontvangen, dan zou 11,3% van de sterfgevallen en/of ernstige aandoeningen vermeden kunnen worden.
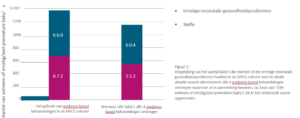
Dit betekent dat hoewel de patiëntkenmerken, zoals de leeftijd van de moeder bij de geboorte, de zwangerschapsduur, het voorkomen van meerlinggeboorten of het voorkomen van pre-eclampsie (ook bekend als ‘zwangerschapsvergiftiging’) per regio verschillen, dit de verschillen in sterfte en gezondheidsproblemen gevonden in verschillende regio’s niet volledig kan verklaren.
→ De bevinding suggereert een bestaande ongelijkheid in de kwaliteit van zorg en behandeling voor extreem of ernstig/zeer premature baby’s binnen Europa.
→ Uit de resultaten blijkt dat sterfte en gezondheidsproblemen minder voorkwamen bij baby’s, die evidence-based behandelingen ontvingen. Verschillen in het gebruik van wetenschappelijk evidence-based zorg in regio’s en afdelingen werden gevonden, b.v. voor hypothermiepreventie (voorkomen van onderkoeling) of het niet-gebruik van corticosteroïden na de geboorte.
→ Deze bevindingen tonen aan dat er nog ruimte is voor verbetering en dat veranderingen in de organisatie en kwaliteit van de geleverde zorg nodig zijn.
Welke zijn de faciliterende en belemmerende factoren om evidence-based zorg en de beste klinische behandelingen in neonatale intensive care-afdelingen te implementeren?
Toen 44 artsen en verpleegkundigen uit 6 EPICE-regio’s werd gevraagd om te vertellen over de laatste verandering in het beleid of de behandelingen die op hun afdeling werden geïntroduceerd, meldden ze de volgende stimulerende en belemmerende factoren:

Wat betekenen deze resultaten?
Het EPICE-project toonde aan dat evidence-based behandelingen niet altijd worden ingezet in de zorg voor extreem of ernstig/zeer premature baby’s in Europa. Belangrijker is dat EPICE aantoonde dat behandelingen, waarvan is aangetoond dat ze effectief zijn in studies, effectief waren in de dagelijkse praktijk, aangezien sterfte en gezondheidsproblemen minder voorkwamen bij baby’s die evidence-based effectieve zorg kregen.
De studie vond ook een grote variabiliteit in het gebruik van sommige interventies op verloskundige en neonatale afdelingen, wat de afwezigheid van een gemeenschappelijke overeenstemming over de beste praktijken onderstreept. Dit toont de noodzaak om de informatie-voorziening van clinici te verbeteren, hetgeen op zijn beurt een beter bewijs vereist voor de behandelingen die nodig zijn om voor deze kwetsbare baby’s te zorgen. De relatie die in deze studie is gevonden tussen de aanwezigheid van specifieke richtlijnen op afdelingen en het percentage waarin dergelijke behandelingen worden uitgevoerd bevestigt het nut van dergelijke richtlijnen. Het is dus belangrijk om onderzoeksresultaten te vertalen in richtlijnen die ondubbelzinnig, duidelijk geschreven en gemakkelijk te interpreteren zijn. Deze moeten wijzen op de voordelen voor patiënten en professionals in de gezondheidszorg.
Gerandomiseerde gecontroleerde studies zijn nodig wanneer er onduidelijkheid bestaat over de werkelijke waarde en voordelen van interventies.
De algemene boodschap van EPICE is dat een beter gebruik van wetenschappelijk evidence-based zorg kan leiden tot aanzienlijke gezondheidsvoordelen voor extreem of ernstig/zeer premature baby’s.
Volgende stappen
EPICE onderzocht hoe evidence-based behandelingen de uitkomst beïnvloedde voor extreem of ernstig/zeer premature baby’s bij de geboorte en tijdens hun ziekenhuisverblijf als pasgeborene. Hoe deze behandelingen van invloed zijn op de ontwikkeling en de gezondheid van vroeggeboren kinderen op lange termijn, wordt momenteel onderzocht in de lopende onderzoeken in de SHIPS en RECAP projecten.
Vooruitzichten
De Europese Stichting voor de Zorg van Pasgeboren Baby’s (EFCNI) ontwikkelt samen met vele deskundigen en oudervertegenwoordigers Europese normen voor gezondheidszorg voor pasgeboren, belangrijke onderwerpen in de gezondheid van pasgeborenen en stelt een standaardkader vast voor het ontwikkelen van richtlijnen op landelijk-, regio- en afdelingsniveau .
Binnen het project Europese Standaarden voor Zorg voor Pasgeborenen wordt het hele scala van problemen in verband met prematuriteit en neonatale gezondheidsproblemen behandeld.
Het multidisciplinaire project combineert meer dan 220 professionals in de gezondheidszorg van verschillende beroepen, oudervertegenwoordigers en geselecteerde specialisten in het veld uit meer dan 35 landen. Vertegenwoordigers van nationale ouderorganisaties spelen een belangrijke rol in alle fasen van het project – van de ontwikkeling tot de implementatie van de standaard.
Alle belanghebbenden kunnen helpen dit referentiekader in hun land te promoten. Zie https://newborn-health-standards.org/ of http://www.efcni.org/ voor meer informatie over het project.
Financiering
Dit project heeft financiering ontvangen van het 7e Kaderprogramma van de Europese Unie onder subsidieovereenkomst nummer 259882.



